Алюминий это металл или неметалл
Один из самых распространенных в строительстве и технике металлов — алюминий. Он используется не только в чистом виде, но и в составе различных сплавов. В земной коре он тоже достаточно широко распространен, занимая почетное третье место, отставая только от кремния и кислорода. Если отдельно взвесить все компоненты, составляющие земную кору, то на алюминий придется 8% от общей массы.
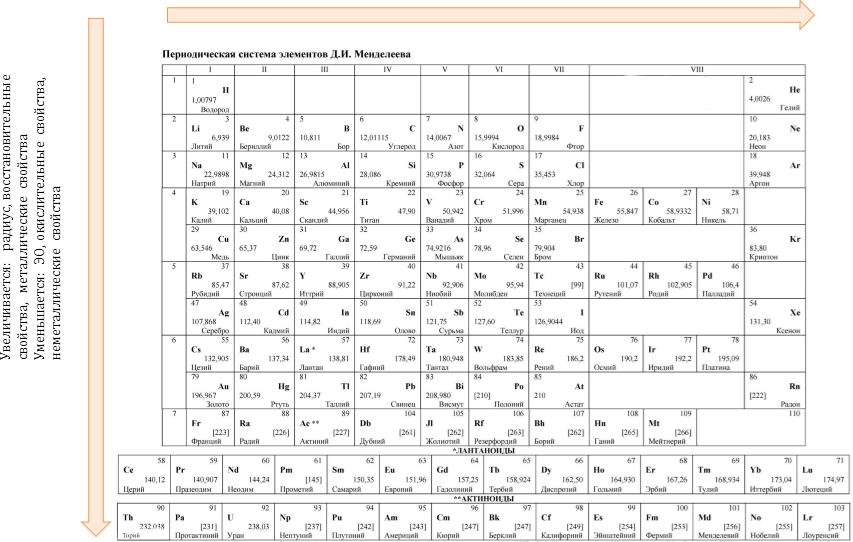
Найти алюминий в периодической системе элементов можно в главной подгруппе III группы, или по новой классификации — в 13 группе. Кто знаком с основами построения таблицы, то безошибочно определит, что этот элемент — металл. В чистом виде найти алюминий не получится, он находится в виде соединений с другими элементами — полевой шпат, квасцы, бокситы, слюда, корунд. Даже в рубинах и сапфирах есть атомы алюминия.
Производится алюминий в промышленных масштабах из бокситов, сначала получают оксид алюминия, сильно нагревая сырье, затем подвергают расплав гидролизу. На катоде оседает металл, на аноде выделяется кислород в виде газа. Фильтрацией или другим способом чистый алюминий получить не удается.
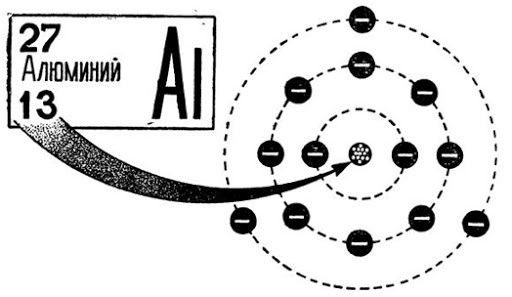
Как устроен атом алюминия
В периодической системе алюминию присвоен 13 номер. В ядре элемента находится 13 нейтронов и 14 протонов. Электронная конфигурация элемента имеет вид 1s22s22p63s23p1, а конфигурация электронного распределения — +13Al)2)8)3. Три электрона из последней орбиты легко отделяются, что определяет высокий уровень окисления +3.
В естественном состоянии чистый алюминий существовать не может, поверхность слитка или изделия сразу же покрывается пленкой окислов, образующих герметичную оболочку. Это объясняет, почему алюминий не реагирует с водой и не поддается коррозии.
Физические и химические свойства алюминия
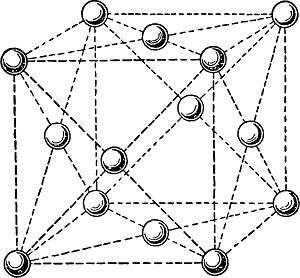
Если рассматривать физические свойства металла, то алюминий обладает небольшой массой, пластичен и хорошо проводит электричество. В нормальных условиях металл мгновенно покрывается защитной пленкой и не вступает в реакцию ни с водой, ни с кислотами. Это определяет популярность алюминиевой тары для транспортировки этих химических веществ. Кристаллическая структура определяет высокую пластичность металла.
Оксидная пленка снимается солями аммония, горячими щелочами и сплавами ртути, после чего металл вступает в реакцию со многими веществами, в частности с галогенами при комнатной температуре, а при нагревании — с фосфором, серой, азотом, углеродом. С водородом в реакцию металл не вступает. Степень окисления алюминия в соединениях всегда +3, в элементарном состоянии — 0.
Применение алюминия
Популярность металла во многом определена еще одним свойством, он не намагничивается. Это позволяет использовать его для изготовления корпусов различных машин, приборов, проводов. Отличная электропроводимость делает алюминий идеальным материалом для производства кабелей.
Алюминий плавиться при температуре 658 0С, в расплаве легко вступает в реакцию с другими элементами, меняя свою структуру и свойства. Сплавы на основе алюминия обладают таким же небольшим весом, но значительно тверже, легче в обработке и долговечнее, чем чистый металл.
Одна из форм использования элемента в технике и быту — алюминиевая пудра. Это измельченный до мелкодисперсного состояния чистый алюминий, смешанный с 3 – 3,5 % жирных веществ. Частицы металла имеют чешуйчатую форму, при использовании пудры в качестве краски, они ложатся плоской стороной на поверхность, создают прочную антикоррозионную защиту и придают изделию декоративный вид.
Кроме чистого алюминия в порошке могут находиться железо, кремний, медь в количестве 0,01 – 0,5%. Это просто примеси, которые не вступают с алюминием в реакцию и не оказывают влияния на свойства пудры. Мелкодисперсный металл также используется при производстве взрывчатки, смесей для фейерверков, газообразующих компонентов легких бетонов.
Алюминаты
В природе часто встречаются соли ортоалюминиевой H3 AlO3 и металюминиевой кислот HAlO2. Это различные вещества, в которых алюминий полностью потерял свои металлические свойства и приобрел новые. Так алюминат натрия NaAlO2 используется в промышленности как протравочный реактив, другие соединения, как добавки для бетонов и растворов, ускоряющее отвердевание и повышающие пластичность. Металлические свойства алюминия в этих соединениях никак не проявляются. Степень окисления алюминия в метаалюминиевой кислоте и солях такой же, как и в оксидах +3.
В природе алюминаты находятся в виде минералов, не зная их химических формул сложно сказать, что в их составе находится один из самых распространенных металлов на Земле. Это минералы шпинель, ганит, герценит, хризоберилл. Сама по себе металюминиевая кислота неустойчива, а вот соли вполне самостоятельные твердые вещества с хорошо выраженными свойствами.